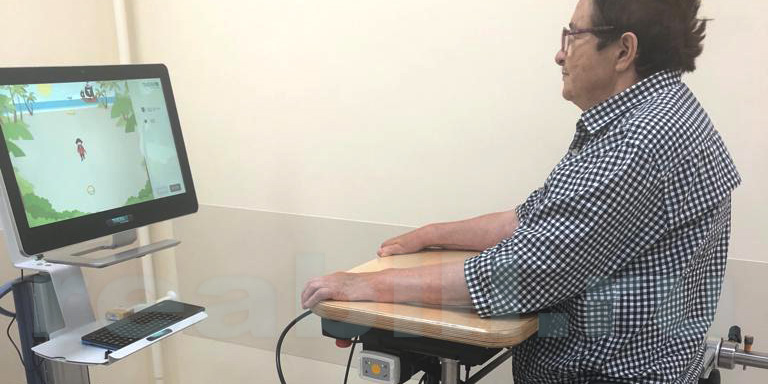
Современная реабилитация больных после инсульта
Инсульт в настоящее время является глобальной медицинской и социальной проблемой в связи с высокими показателями заболеваемости, смертности и инвалидизации.
Введение
В экономически развитых странах смертность от инсульта занимает 2 – 3 место в структуре общей смертности, и составляет 60 – 80 человек на 100 000 населения в год. Наиболее тяжелыми последствиями ишемического инсульта являются центральные параличи, значительно снижающие качество жизни больных [1, 2]. Разработка инновационных немедикаментозных технологий реабилитации больных с наиболее важными в социальном плане заболеваниями является одной из приоритетных задач медицинской науки и практического здравоохранения и важной составляющей Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», № 323-ФЗ от 21.11.2011 г. и Госпрограммы развития здравоохранения РФ до 2025 года, утвержденной правительством РФ 24.12.2012 г. В связи с этим, в последние годы все большее внимание при восстановлении двигательных функций уделяется внедрению роботизированных реабилитационных комплексов, работающих в режиме биологической обратной связи [2, 3]. Одна из ключевых задач трехэтапной реабилитации заключается в определении реабилитационного потенциала пациента и выявления инструментальных предикторов эффективности различных программ реабилитации [3 – 6].
Цель исследования
Оценить возможность использования комплекса нейрофизиологических методов (вызванные потенциалы и транскраниальная магнитная стимуляция) в качестве предикторов эффективности восстановления нарушенных двигательных функций у больных с ишемическим инсультом под влиянием роботизированной механотерапии.
Материал и методы исследования
В период с 2006 по 2013 год обследовано 628 пациентов (346 мужчин и 282 женщины) в возрасте от 47 до 72 лет (средний возраст 51,4±1,23 года), госпитализированных к нам в первые сутки развития ишемического инсульта в бассейне средней мозговой артерии. Распределение пациентов на основную (n=312) и контрольную (n=316) группы было проведено с применением последовательной рандомизации.
Пациентам основной группы (n=312) проводилась стандартизированная трехэтапная реабилитация (медикаментозная терапия, массаж, лечебная гимнастика, тренировки на циклических тренажерах, физиотерапия, функциональная электростимуляция) с включением на 1-м и 2-м этапах роботизированной механотерапии (Эриго и Локомат). Программы реабилитации пациентов контрольной группы (n=223) отличались лишь по одному компоненту – отсутствию в них роботизированной механотерапии.
Клиническая картина оценивалась по жалобам, анамнезу, соматическому и неврологическому статусу c балльной оценкой по шкале NIHSS. Мобильность пациента и уровень активности оценивались с помощью индексов Хаузера, Ривермид и Бартел.
Изучение функции моторной и сенсорной коры в процессе восстановления проводилось методом транскраниальной магнитной стимуляции (ТКМС) и методом анализа соматосенсорных вызванных потенциалов (ССВП). Регистрация получаемых ответов проводилась на электромиографе «Нейро-МВП-Микро» («Нейрософт, Россия). Стимуляция проводилась магнитным стимулятором «Нейро-МС» («Нейрософт», Россия) с использованием большого кольцевого индуктора. Оценивалась амплитуда вызванного моторного ответа (ВМО) при корковой стимуляции, межамплитудный коэффициент (МАК), время центрального моторного проведения (ВЦМП). Комплексное клинико-инструментальное обследование проводили на 21 и 42-й день непрерывной реабилитации и в отдаленном периоде – через 6 месяцев.
Статистический анализ полученных результатов проводился с помощью пакета прикладных компьютерных программ SPSS 10.0. Достоверность различий средних значений полученных показателей определялась с помощью критерия Стьюдента, частоты встречаемости признака – по точному методу Фишера, а изменения характера распределений значений того или иного параметра – с помощью критерия χ2 Пирсона. Для оценки предикторов эффективности медицинской реабилитации проводился корреляционный, дисперсионный и регрессионный анализы.
Результаты исследования и их обсуждение
В день госпитализации тяжесть инсульта по шкале NIHSS составляла 18,5±0,13 балла. По степени выраженности пареза все больные были разделены на три группы: 22,7% пациентов с грубым парезом (1,60±0,03 балла), 44,6% с выраженным парезом (2,50±0,04 балла) и 32,7% пациентов с умеренным парезом (3,45±0,06 балла). В группе контроля было 21,4%, 43,2% и 35,4% пациентов соответственно, со средними значениями 1,52±0,06; 2,51±0,11; 3,42±0,13 балла.
При нейрофизиологическом исследовании оказалось, что у всех пациентов с ишемическим инсультом до начала лечения при стимуляции над пораженным полушарием ответ с мышцы был значительно снижен или отсутствовал.
Дополнительно пациентам проводилось исследование ССВП. При этом учитывалась латентность пика N20 (ответ первичной сенсорной коры) и амплитуда коркового ответа.
После каждого этапа реабилитации отмечено уменьшение тяжести инсульта по Шкале NIHSS с достоверно значимым (p<0,05) различием между основной и контрольной группами.
Мобильность по шкале Ривермид на 21-е сутки у пациентов основной группы была выше на 10,5% по сравнению с группой контроля. К моменту выписки из стационара (42-е сутки) это превышение составило уже 95,3%, а через 6 месяцев – 27,4%, то есть достоверно значимое различие функциональных исходов между группами зарегистрировано на всех этапах реабилитации. Показатели бытовой активности по шкале Бартел претерпели аналогичные изменения.
На 21-е сутки курса ранней реабилитации отмечалось достоверно значимое увеличение мышечной силы в паретичной нижней конечности независимо от тяжести центрального пареза. У пациентов группы контроля снижение степени пареза в паретичной нижней конечности было достоверным только в случае умеренного пареза, при грубой и выраженной степени позитивные изменения не были достоверно значимыми. Иной была динамика снижения степени пареза в паретичной верхней конечности. На 21 сутки отмечалось достоверно значимое снижение умеренного или выраженного пареза как в основной, так и в контрольной группе и отсутствие значимой динамики в случае грубого пареза у больных обеих групп.
После курса роботизированной механотерапии на комплексе Локомат, проводимого в раннем восстановительном периоде ишемического инсульта, отмечено дальнейшее снижение пареза в ноге у больных с центральным параличом. При этом достоверно значимое (p<0,05) межгрупповое различие зарегистрировано у пациентов с умеренным и выраженным парезом. Под воздействием локомоторных занятий на комплексе Локомат не было отмечено более значимого восстановления движений в верхней конечности по сравнению с группой контроля.
Через 6 месяцев после начала исследования отмечено дальнейшее снижение степени пареза в нижней конечности с достоверно значимым межгрупповым различием только у пациентов с умеренным парезом в дебюте заболевания. В случае более тяжелых двигательных расстройств преимущества использования ассистирующих роботов через 6 месяцев после ишемического инсульта не выявлено. Отмечалось уменьшение степени пареза верхней конечности у пациентов основной и контрольной групп без достоверно значимых различий между группами.
В качестве основного признака, отражающего активность моторной коры, был выбран межамплитудный коэффициент (МАК), который показывает возбудимость коры и оставшееся количество моторных элементов. Достоверно значимые изменения МАК отмечены у пациентов основной группы на 42-е сутки реабилитации и в отдаленном периоде (через 6 месяцев). В группе контроля изменения МАК были позитивными, но без достоверной значимости. Аналогичные изменения с достоверной значимостью у пациентов основной группы претерпели показатели амплитуды коркового ответа P18-N20 и латентности пика N20.
Анализ предикторов эффективности применения различных методов реабилитации пациентов с ишемическими инсультом был проведен с использованием специальных методов статистического анализа, включавших алгоритмы анализа дисперсий, корреляционный анализ и регрессионные модели.
Проведению регрессионного анализа предшествовала процедура нормирования и центрирования показателей, что делает более информативными коэффициенты регрессионного уравнения, которые в этом случае дают более полное представление о доли влияния того или иного показателя в общей картине благоприятной динамики состояния пациента в процессе лечения. Проведение множественного регрессионного анализа позволило установить ряд закономерностей.
Подтвердилась известная закономерность о важной роли таких параметров как тяжесть инсульта, выраженность пареза, активность моторной коры при ТКМС, как прогностических факторов, определяющих скорость восстановления нарушенных функций. Также необходимо подчеркнуть, что более молодые пациенты в плане эффективности лечения имели небольшое преимущество перед остальными, что лишний раз свидетельствует о более высокой активности нейропластических процессов.
Для того чтобы статистически оценить эффективность предикторов, мы были вынуждены сократить число результирующих признаков до разумного минимума и выбрали наиболее значимые из них: это мобильность по шкале Ривермид и бытовая активность по шкале Бартел. В качестве предиктора был выбран кроме параметров регрессионного уравнения также возраст пациентов. Установлено, что эффективность реабилитации в основном определяется тяжестью инсульта, выраженностью пареза и активностью моторной коры.
Выводы
Установлено, что максимальное повышение эффективности медицинской реабилитации, обусловленное использованием роботизированной механотерапии, зависит при инсульте от таких прогностических факторов как тяжесть инсульта, выраженность пареза и активность моторной коры при ТКМС, доля влияния которых на эффективность медицинской реабилитации достигает 79%, с точностью прогноза от 68 до 96%. Предложенный комплексный клинико-нейрофизиологический подход может быть использован для определения реабилитационного потенциала пациентов с ишемическим инсультом.
Список литературы
1. Даминов В.Д., Кучеренко С.С., Сагильдина Ю.О., Кузнецов А.Н. Роботизированные технологии в реабилитации больных после хирургической реваскуляризации мозга// Вестник восстановительной медицины. -2012. - № 2. -С. 29-32.
2. Даминов В.Д. Роботизированная локомоторная терапия в нейрореабилитации// Вестник восстановительной медицины. -2012. - №1. -С.57-62.
3. Иванова Г.Е. Медицинская реабилитация в России. Перспективы развития. // Вестник восстановительной медицины. -2013. - № 5. -С.3-8.
4. Короткова И.С., Уварова О.А., Даминов В.Д. Комплексный мониторинг эффективности нейрореабилитации // Материалы I международного конгресса «Нейрореабилитация 2009». -М., 2009. -С. 10.
5. Бобровницкий И.П., Лебедева О.Д., Яковлев М.Ю. Применение аппаратно-программного комплекса оценки функциональных резервов для анализа эффективности лечения //Вестник восстановительной медицины.-2011.-No6.-с.7-9
6. Бобровницкий И.П., Василенко А.М., Нагорнев С.Н., Татаринова Л.В., Яковлев М.Ю. Персонализированная восстановительная медицина: фундаментальные и прикладные подходы к медицинской реабилитации и нелекарственной профилактике // Russian journal of rehabilitation Medicine. – 2012, No1. – С. 9-20.
Контакты:
Даминов Вадим Дамирович. E-mail – daminov07@mail.ru
